Literární zdroje uvádějí, že na SARS-CoV-2 je ve světě již v běhu příprava více než 120 vakcín. Jedna z nich nazvaná NVX-CoV2373 by se měla dokonce vyrábět v továrně v Bohumili (mezi Prahou a Kolínem). Tu ale za „naší“ považovat nemůžeme, protože jde o podnik americké společnosti Novavax. Na vývoj údajně měla k dispozici miliardy dolarů (naše vláda hodlá na vývoj české vakcíny uvolnit několik milionů, korun). Přesto Novavax asi nebude mezi prvními výrobci, kteří vakcínu budou schopni dodat na trh. Podle dostupných údajů by nadnárodní společnost AstraZeneca měla být zhruba o půl roku rychlejší.

Zatímco v našem (českém případě) má jít o takzvanou inaktivovanou vakcínu, která obsahuje usmrcené viry (respektive jejich části), konkurence většinou sází na vakcíny v nichž se využívá jen konkrétní imunogenní glykoproteinová molekula. Takové vakcíny jsou považovány za „šetrnější“, neboť nezatěžují imunitní buňky tvořením protilátek proti něčemu, co není pro šíření viru tak důležité a co lze považovat za zbytečné plýtvání schopnostmi imunitního systému k tvorbě kromě žádoucích substancí, i jakéhosi „balastu“.
V květnu, kdy se náš výzkum nacházel v první (laboratorní fázi), u podobné vakcíny vyvíjené rovněž na bázi inaktivovaného viru, již Čína hlásila zahájení klinických testů s vakcínou BBIBP-CorV vyvíjenou jejich domácí společností Sinopharm. Ze zveřejněné zprávy vyplývá, že jejich vakcína chrání před nákazou jak hlodavce (myši, morčata, potkany), tak i primáty (makaky). Pokusná zvířata neonemocněla ani když jim následně podali vysoké dávky infekčního viru. Kromě této zmíněné vakcíny má Čína v klinických testech ještě další dvě želízka v ohni. Mnozí odborníci za světového lídra v závodech o první místo vakcíny dodané na trh tipují čínskou společnost: CanSino Biologics. Ta vyvíjí rekombinantní vakcínu SARS-CoV-2 na bázi adenoviru typu 5 (Ad5-nCoV).
Z včera zveřejněných informací v prestižním časopisu New England Journal of Medicine vyplývá, že s přípravou syntetické vakcíny jsou přinejmenším stejně daleko jako v Číně, i v Americe u společnosti Moderna. Té se od americké vlády dostalo podpory v podobě finanční injekce téměř pěti set milionů dolarů. V Americe vyvíjená vakcína s pracovním názvem mRNA-1273 se již koncem května dostala do druhé fáze klinických testů (na lidech) a tento měsíc podstupuje již třetí fázi testů. Mělo by jít o takzvanou „messenger RNA vakcínu“. Protože u ní vše vychází velmi nadějně, nebude na škodu si trošku přiblížit, o co v jejím případě jde.
Musíme zabrousit do počátku devadesátých let, kdy si vědci na myších vyzkoušeli do té doby teoretickou možnost přímé injekce nukleových kyselin (RNA nebo DNA) do svalu za účelem tvorby proteinu, který dodaná nukleová kyselina kóduje. Pokusy na myších tehdy ukázaly, že teorie funguje a že místo toho, aby se do svalu píchal inaktivovaný virus (nebo část jeho proteinové obálky), stačí dodat pouze sekvenci, která kóduje protein patogenu. Jinými slovy, vpravuje se do svalu pouze pokyn pro tvorbu proteinu, proti němuž chceme aby si imunitní systém vytvořil imunitu. Tento typ vakcinace lze provádět jak pomocí DNA sekvence, tak i RNA kódu. Zvolená molekula (ať už DNA, nebo RNA) kódující protein patogenu, se vpravuje do buněk ve formě krátké cirkulární molekuly – tzv. plazmidem. V případě firmy Moderna a jí připravovanou vakcíny, jde o pokyn zapsaný do řetězce RNA. To je ta lepší volba z obou zmíněných variant. U DNA vakcíny přece jen existuje jisté riziko, že by se vkládaný DNA řetězec mohl zabudovat do genomu pacienta na nějaké nevhodné místo, kde by pak dělal neplechu.U RNA vakcíny nic takového nehrozí, neboť nukleová kyselina neproniká do jádra buňky. Vše potřebné, na čemž závisí tvorba provokujícího proteinu, se odehrává v cytoplazmě.
Nutno dodat, že počáteční nadšení, že se novým způsobem začnou vyrábět vakcíny jak na běžícím pásu, zhatily klinické studie. Většinou byly zklamáním. Na vině byla malá stabilita vkládaných krátkých RNA molekul. Teprve až v poslední době vědci přicházejí na to, jak vylepšit stabilitu vkládané mRNA a čím se dá produkce zamýšlených proteinů zlepšit. Lze na to jít dvěma cestami. Jedna využívá toho, že se nukleosidy modifikují, čímž se buňkám nedaří je tak tak snadno „rozebrat“ a odstranit. Druhý způsob využívá navázání RNA molekul na nanočástice. Pokud se zvolí ten správný materiál (například vhodné lipidy), rovněž dojde ke stabilizaci RNA molekuly a navíc se tím ještě zvýší ochota buněk nechat si RNA proniknout přes membránu do svého nitra. Do třetice se dá nanočásticemi vylepšit i to, čemu se říká biologická dostupnost vkládané RNA. Tímto termínem se označuje, když podvrženou informaci cytoplazmatický aparát ochotněji zpracovává a buňka produkuje požadovaného patogenního proteinu víc. Že se to odrazí na vlivu na bílé krvinky a množství jimi produkovaných protilátek, je zbytečné rozvádět.
Když se to vše pokusíme shrnout, tak v případě společnosti Moderna jde o navození imunity pomocí syntetické RNA vakcíny, kdy se hostitelské buňky přinutí k replikaci a translaci exogenní RNA kódující vakcinační antigen. Polopaticky řečeno, podle dodaného genetického kódu si tělo vyrobí kousek patogenu a proti němu si imunitní systém vyrobí protilátky. A až se setkáme s kovidem, nedáme mu šanci. Dál už šermovat termíny transfekce, amplifikace, translace, nebudeme a raději si povíme, jak daleko se s vakcínou už vědci dostali.
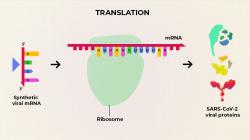
Publikované výsledky nasvědčují tomu, že kandidátní molekulou na vakcínu „mRNA-1273“ imunogenetici trefili do černého. Jednak proto, že látka je lidmi obecně dobře tolerována. A co je důležitější, zajišťuje to, co se od ní očekává – navozuje u pokusných osob tvorbu virus neutralizačních protilátek. V nejnovějším čísle časopisu The New England Journal of Medicine vědci z Moderna, Inc. v Cambridge, Massachusetts a jejich kolegové z Národního institutu pro alergické a infekční choroby (NIAID) odbornou mluvou popsali, jak se jim syntetickou molekulu kódující antigen z glykoproteinu transmembránové kotvy a neporušeného štěpícího místa podařilo připravit. Laicky řečeno, injekcí RNA molekul navozují proces, který vyústí v tvorbu protilátek namířených na část proteinu, kterou má koronavirus na svých výčnělcích a jimiž se na lidské buňky přichycuje (proto si nemůže dovolit v něm moc experimentovat s mutacemi). Vyřazením této virové struktury protilátkou z něj dělá partikuli neschopnou lézt nám do buněk. A to je to, o co nám u vakcinace jde.
V publikaci se uvádí, že první účastník pokusu obdržel zobanec s experimentální vakcínou už 16. března a že pokusy vede Lisa A. Jacksonová z Kaiser Permanente Washington Health Research Institute v Seattlu. Krátce po prvním odvážlivci následovalo dalších 44 dobrovolníků ve věku 18 až 55 let. Dostali dvě intramuskulární injekce (druhou 28 dnů po té první). Zkoušelo se dávkování 25, 100 nebo 250 mikrogramů vakcíny. V dubnu probíhající pokusy rozšířily osoby starší 55 let a nyní je v pokusu již 120 osob. Vyhodnocena mohla být zatím ale jen věková skupina 18 až 55 let. Výsledky jsou následující: Zhruba u poloviny osob vakcinace přivodila běžné vakcinační stavy, jako jsou únava, bolest hlavy, zimnice, nebo bolest v místě vpichu. Žádné závažné vedlejší účinky nebyly pozorovány.
Nyní to nejdůležitější: Měření hladiny neutralizační aktivity navozené vakcínou (po druhé injekci) ukázaly, že dobrovolníkům v krvi začaly kolovat virus neutralizující protilátky. Jejich množství (charakterizované titrem) se pohybovalo nad průměrem pozorovaným v séru rekonvalescentů s potvrzenou chorobou COVID-19.
Proč se hovoří o úspěchu, když korelace ochrany před infekcí SARS-CoV-2 ještě nebyly u vakcíny stanoveny? Dovoluje to měření sérové neutralizační aktivity, která je uznávaným korelátem ochrany pro respirační viry, jako je chřipka, nebo respirační syncytiální virus. Neutralizační aktivita je obecně přijímána jako funkční biomarker humorální odpovědi in vivo. Podle imunologů vakcinovaným už COVID-19 nehrozí. Druhá fáze klinického hodnocení mRNA-1273 začala na konci května a nyní již by měly být v běhu zkoušky účinnosti fáze 3. Ty se prakticky dělají už jen s cílem vyloučit nějaké případné vedlejší účinky. Včera zveřejněné výsledky jsou natolik slibné, že z nich lze usoudit, že účinná vakcína, se objeví na trhu mnohem dříve, než se předpokládalo.
Literatura
Lisa A. Jackson et al, An mRNA Vaccine against SARS-CoV-2—Preliminary Report, New England Journal of Medicine (2020). DOI: 10.1056/NEJMoa2022483
Diskuze:




