Pojem „covid“, který ne tak dávno byl jedním z nejčastěji používaných slov v naší komunikaci a asi se slovem „dolar“ tím nejčastějším z mezinárodního hlediska, se z ní rychle vytrácí. Naštěstí. Nicméně se k této, před třemi i dvěma lety tak obávané viróze v několika řádcích vraťme. Na internetových stránkách nejnovějšího čísla časopisu NATURE najdeme volně dostupný článek 39členného americko-australského týmu s výmluvným názvem Běžně se vyskytující alela HLA je spojena s asymptomatickým průběhem infekce SARS-CoV-2 (A common allele of HLA is associated with asymptomatic SARS-CoV-2 infection).
Autoři v něm zveřejnili výsledky pátrání po souvislostech mezi bezpříznakovým průběhem infekce a mutacemi v genech HLA (Human Leucocyte Antigen), které kódují tvorbu určitých peptidů – bílkovinám podobných molekul, jen s kratším řetězcem aminokyselin.
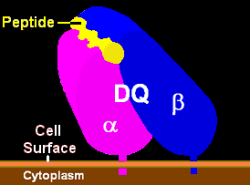
Když je buňka napadena virem, jeho části (fragmenty) vystaví HLA systém pomocí těchto peptidů na povrchu vnější membrány, kde stopy vetřelce rozeznají imunitní T-lymfocyty a celou buňku zničí. Takovým signálním antigenem může být například část známého spike proteinu koronaviru. Jakéhokoli koronaviru. Napadena buňka změní konformaci proteinů na své membráně a dává svému okolí na vědomí, že se s ní něco děje. Do akce vstupují buňky zvané pomocné buňky (helper cells), které zabíječským T-lymfocytům ukážou, co by je mělo zajímat a na co mají útočit. Takto poučené T-lymfocyty jsou schopny s označenou buňkou skoncovat. Zda k rozpoznání, a tedy k útoku na nájezdníkem zotročené buňky dojde, tedy rozhodují jemné změny v peptidech se stopami vetřelce. Vše je řízeno návodem, který mají buňky ve své jádrové DNA, v genech HLA, od jejichž mutací pak závisí přesné složení a s ním související 3D struktura jimi kódovaných peptidů, jež pak mohou být více, nebo méně „účinné“. To je tajemství souvislosti, kterou objevili autoři studie – souvislosti mezi velice lehkým průběhem nemoci a jistou formou HLA genů.
Tato důmyslná obrana může však mít problém při reakci na zcela nový patogen. T-lymfocyty, jež jsou klíčové v mechanizmu specifické (získané) buněčné imunity (viz video pod textem) jsou druhem bílých krvinek. Vznikají v kostní dřeni, třídí se a dozrávají v brzlíku, kde se učí rozeznávat HLA systémy vlastních buněk a antigeny nebezpečných vetřelců. Na ty nové, tělu doposud neznámé, se musí nejdřív vycvičit.
Vědci pomocí analýzy dostupných údajů z databáze dárců kostní dřeně, kteří si prošli COVIDem-19 zjistili, že relativně rozšířená mutace HLA, označena jako HLA-B*15:01, vyskytující se u 10 % obyvatel USA s evropskými předky, pomohla svým nositelům překonat nákazu bez příznaků. Kdo ji zdědil jenom po jednom z rodičů (je pro danou alelu heterozygotem) měl při pandemii dvakrát vyšší šanci asymptomatického průběhu než lidé porovnatelného věku a zdravotního stavu s jinou formou příslušného HLA genu. Homozygotní nositelé, jež mutaci zdědili od obou rodičů, měli až 8x vyšší pravděpodobnost, že si nákazu v podstatě ani nevšimnou. Tento, pro samotné nositele příslušné alely pozitivní fakt měl i svou negativní stránku – netušené nákazy přispěly k šíření COVIDu, zejména jeho varianty delta.
To, že se výsledky týkají zejména lidí evropského původu není projevem nějaké diskriminace, ale důsledkem údajů, které měli vědci k dispozici. Databáze dárců kostní dřeně jim poskytla potřebné HLA genetické profily, ale jen do ní zařazených dobrovolníků. Z nich vybrali téměř 30 000 lidí, u nichž pak zjišťovali, jaké měli výsledky testů na COVID a všechny příznaky v případě jejich pozitivity. Z více než 1 400 účastníků, kterým testy prokázaly nákazu v době, kdy ještě nebyly dostupné vakcíny, tedy jejich imunitní systém ani průběh nemoci nebyly ovlivněny očkováním, 136 lidí překonalo COVID-19 bez příznaků.
##seznam_reklama##
Jak může nějaká mutace v HLA genu přispět k lepší imunitní ochraně? Vědci to vysvětlují lepší takzvanou křížovou imunitou. Virus SARS-CoV-2 byl pro všechny nakažené neznámý, nicméně jeho spike protein se podobá spike proteinům jiných koronavirů způsobujících obvyklá sezónní nachlazení. Jejich šíření je v našich populacích zcela běžné, znají to zejména rodiče dětí předškolního věku. Na tyto koronaviry imunitní systém téměř všech lidí dokáže reagovat a útočníka bez závažnějších důsledků eliminovat. V případě alespoň jedné „ochranné“ mutace HLA (alely HLA-B*15:01) prý dochází k prezentaci fragmentu spike-proteinu SARS-CoV-2 na povrchu napadené buňky způsobem, který T-lymfocytům více připomíná fragmenty spike proteinů běžných koronavirů a tím nastartuje rychlejší a silnější imunitní odezvu.
Video o našem imunitním systému v kostce. Krátké, srozumitelné, názorné, vtipně zpracované:
Literatura:
Pro laiky, kteří by systému adaptivní imunity chtěli o něco lépe porozumět:
Video: Buněčná imunita – Adaptivní imunita
Překlad titulků:
Adaptivní imunitní reakce, známá také jako získaná nebo specifická imunita, je obranný systém těla přizpůsobený konkrétnímu patogenu. Má dvě větve: buněčnou neboli buňkami zprostředkovanou imunitu a humorální neboli protilátkami zprostředkovanou imunitu. Hlavními účastníky buněčné imunity jsou T-lymfocyty. Vyvíjejí se v brzlíku, podle něhož jsou pojmenovány. Během procesu dozrávání vznikají miliardy variant T-lymfocytů, z nichž každá je nositelem svého jedinečného povrchového proteinu, který se nazývá T-buněčný receptor, TCR. Kromě toho má populace T-buněk, nazývaná pomocné T-buňky, také receptor s názvem CD4, zatímco druhá populace cytotoxických T-buněk nese receptor CD8. V průběhu vývoje se T-buňky také učí nereagovat na tělu vlastní antigeny; ty, které reagují na vlastní molekuly, jsou eliminovány. Zralé T-buňky pak migrují do lymfatických uzlin a dalších lymfatických tkání, kde čekají na vystavení patogenům. Specifická imunita v podstatě spočívá v tom, že napadající patogen najde mezi těmito miliardami variant T-buněk shodu. Selektivně se aktivují pouze ty, které se mohou na patogen navázat. T-lymfocyty však nemohou vázat volně se pohybující patogeny. Mohou se vázat pouze na části patogenu připojené na určitou molekulu hostitele zvanou hlavní histokompatibilní komplex neboli MHC na povrchu tzv. antigen-prezentujících buněk.
Existují dvě třídy MHC:
- Molekuly MHC I. třídy jsou exprimovány všemi jadernými buňkami těla. Tyto molekuly jsou neustále produkovány v cytoplazmě a na své cestě k buněčné membráně zachycují kousky peptidů a zobrazují je na povrchu buňky. Pokud je buňka infikována virem nebo je nádorová, zobrazí se cizí nebo abnormální antigen a buňka se může navázat a aktivovat odpovídající T-buňku. MHC-I váže pouze receptor CD8, čímž aktivuje pouze cytotoxické T-buňky.
- Molekuly MHC II. třídy se vyskytují výhradně na speciálních antigen prezentujících buňkách, z nichž nejúčinnější jsou dendritické buňky. Rezidentní dendritické buňky v místě infekce pohltí patogeny, rozřežou je na kousky a zobrazí je na molekulách MHC-II na svém povrchu. Tyto dendritické buňky pak migrují do nejbližší lymfatické uzliny, kde prezentují antigeny odpovídající pomocné T-buňce, jejíž receptor CD4 se váže na MHC-II. Aktivace T-buněk však vyžaduje druhou vazbu mezi oběma buňkami. Jedná se o ověřovací krok a tento ochranný mechanismus slouží k tomu, aby imunitní systém nereagoval přehnaně. Po aktivaci procházejí T-buňky opakovanými cykly mitózy v procesu zvaném klonální expanze. Tento proces vytváří klony identických cytotoxických a pomocných T-buněk, které jsou specifické pro daný patogen. Některé z těchto buněk se diferencují v efektorové buňky, zatímco jiné se stávají paměťovými buňkami. Většina efektorových T-buněk se z lymfatické uzliny dostane do krevního řečiště a je dopravena do místa infekce, kde provede imunitní útok proti patogenu. Pomocné T-buňky produkují interleukiny, které pomáhají s aktivací cytotoxických T-lymfocytů, B-lymfocytů a dalších imunitních buněk. Pomocné T-lymfocyty mají díky svým rozmanitým funkcím zásadní význam pro adaptivní imunitu. Cytotoxické T-lymfocyty jsou naopak hlavními aktéry buněčné imunity. Uvolňují toxiny a přímo zabíjejí infikované nebo rakovinné buňky. Zatímco efektorové buňky umírají během infekce nebo krátce po ní, paměťové buňky žijí mnohem déle. Některé z nich zůstávají v lymfatických uzlinách, zatímco jiné kolují v krvi nebo migrují do periferních tkání. Paměťové T-buňky jsou také početnější než původní naivní T-buňky. Při opětovném vystavení stejnému patogenu mohou vyvolat mnohem rychlejší imunitní odpověď a zničit patogen tak rychle, že nejsou patrné žádné příznaky nemoci. Je důležité si uvědomit úlohu třetí populace T-buněk, známé jako regulační nebo supresorové T- buňky, jež tlumí imunitní odpověď, když už není potřeba. Jakmile je patogen odstraněn, regulační T-buňky snižují proliferaci efektorových T-lymfocytů a brání tak imunitní reakci, aby se vymkla kontrole. Pomáhají také rozlišovat mezi vlastními a cizími antigeny, a tím předcházet autoimunitním onemocněním.
Video: Humorální imunita