Kolektiv autorů z Howard Hughes Medical Institute, pod vedením Xiaodong Wanga, publikoval v časopise Cancer Cell práci, která se věnuje problematice poškozených buněk. Poničené buňky, jak známo, spouští jemně balancované procesy, které známe pod označením apoptóza a programovaná smrt.
Co je to Smac
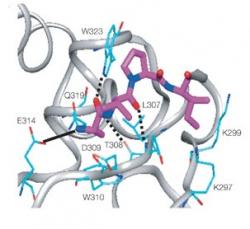
Smac je zkratka pro molekulu aktivní látky, která se celým jménem nazývá „Second mitochondria-derived activator of caspase“. Jde tedy o protein, který tvoří mitochondrie a který aktivuje enzym kaspázu. Slovo aktivátor symbolizuje fakt, že tato molekula stojí na začátku kaskády metabolických pochodů zasahujících do procesu apoptózy. Jakmile je jednou Smac z mitochondrií uvolněn, čeká buňku smrt.
Toto naše vybavení apoptózou je pojistkou proti množení buněk mrzáků, nebo buněk z nějakého jiného důvodu pro tělo nepotřebných. Jde o velmi důležitou funkci. Zajišťuje nám, aby tělo zůstávalo zdravé a nemuselo živit darmožrouty. Problém je v tom, že nádorové buňky se naučily signál vysílaný proteinem Smac, oblafnout. Dokáží ho „vypnout“. Po takovém vypnutí pochopitelně nenastanou ani všechny další potřebné procesy, program řízené smrti selže. Nekontrolovanému množení pak nestojí nic v cestě, máme rakovinu.
Jak jsme si řekli, aktivační impuls dává buňce protein Smac. Studovat vliv proteinu v buňce je ale problém. Není jednoduché jej syntetizovat, uchovat a ani jej nejde do buňky snadno nacpat, tehdy kdy to zrovna potřebujeme. Za tím účelem se Wangův tým uchýlil k malé lsti. Použil takzvané mimetikum. Mimetik je hodně a jsou látky, které se tváří že jsou něco, co nejsou. V tomto případě se jedná o malou syntetickou molekulu, která dokáže spustit enzym kaspázu. Dokáže tedy totéž co protein Smac.

Wang vyvinul molekulu, která je dost malá na to, že jí nedělá problém snadno pronikat do buněk a která přesto umí zmíněný startovací signál napodobit. Toto šidítko tedy buňka vnímá stejně jako signály od skutečného proteinu Smac a začne postupovat podle vnitřního předem určeného plánu vedoucímho k sebe destrukci. Buňka k tomu nepotřebuje asistenci mitochondrií a ani jejich Smac proteinu.
Při pokusech na tkáňových kulturách se ukázalo, že nádorové buňky nejsou žádní hlupáci a že tyto napodobeniny u nich fungují, jen když jsou aplikovány současně ve spojení s další komponentou smrtící mašinérie, známou pod označením TNF-alfa. Pod touto zkomoleninou se neskrývá nic jiného než starý známý zprostředkovatel zánětu.V literatuře se s ním setkáte také pod označením „tumor nekrotizující faktor alfa“ a nebo na webech, kterým se „alfa“ nezamlouvá, jen jako „TNFá“.
Teprve nyní se dostáváme k meritu věci nové studie. Jde o zjištění faktu, že významná část z buněčných linií lidských rakovinových buněk plicní tkáně je citlivá na ošetření pouze samotnou napodobeninou signálu Smac. Když Wang lidské rakovinové buňky vnesl do pokusných myší, začala v nich bujet „lidská“ rakovina plic. Poté, co myším podal své malé molekuly – ony imitace Smac proteinu, nádory se myším zmenšily a nebo vymizely.
To je dost překvapivé zjištění, protože až dosud bylo tyto rakovinné buňky, těžké zabít. Jak se ale také ukázalo, nefunguje to u všech typů nádorů. Dalšími pokusy vyšlo najevo, že na tento druh léčby reagují jen linie nádorových buněk, které si samy produkují vlastní TNF-alfa. Z našeho pohledu jsou takto vybavené nádorové buňky jakoby předem předpřipraveny k snadnějšímu vyvolání apoptózy pomocí imitace napodobující Smac protein.
Paradoxní na tom všem je to, že TNF-alfa je částí metabolické cesty, která propůjčuje nádorům onu mysteriózní schopnost přežít, neboť právě TNF-alfa je pro zvrhlé buňky oním signálem burcujícím je k využití svých růstových schopností a přikazuje jim „množit se, množit se, množit se“.
Kromě zmíněných nádorových buněk z plic jsou na napodobeninu Smac citlivé i některé linie nádorových buněk způsobujících rakovinu prsu a dokonce některé typy buněk způsobujících melanom. To jenom podtrhuje známý fakt, že ne všechny rakoviny plic jsou stejné a že existuje více typů rakovin prsu i melanomů.
V boji s nepřítelem je výhodou když jej dobře poznáte. Z Wangových poznatků vyplývá, že u nádorových buněk, jež si tvoří TNF-alfa, můžeme to, co je předností těchto buněk(umožňuje jim nekontrolovaný růst), využít proti nim. Wangův tým dokázal, že signál k „přežití“ u těchto buněk lze pomocí napodobeniny proteinu Smac vypnout a přepnout ho do polohy „smrt“. Wangův tým je tedy schopen některým nádorům značně ztrpčovat život. A umí to udělat jednoduchou malou molekulou, jejíž syntéza stojí pakatel. Wang dokonce umí předem určit, které nádory na tento druh léčby budou citlivé. Ať už se jedná o nádor plic, mléčné žlázy nebo kůže, vždy půjde o nádory, jejichž buňky se prozradí produkcí TNF-alfa. Na ty bude léčba mimetikem zabírat.
Lidé se již dlouho snaží o přemlouvání nádorových buněk, aby se vrátily na svůj původní, správný, směr - na cestu své programované smrti. Nyní se Wangovu kolektivu podařilo najít správný přepínač a také odhalit, jak ho přepnout. Z tohoto pohledu se výzkum molekul imitujících funkci proteinu Smac jeví jako velmi nadějná cesta k léčbě určitých typů nádorových onemocnění plic, prsu, melanomu a možná i dalších lidských sužovatelů. Půjde přitom o léčbu, která ve srovnání se stávající chemoterapií, bude méně škodlivá.
Pramen: Howard Hughes Medical Institute
