Každé tři sekundy přibyde na světě člověk s diagnostikovanou demencí. Počet takto postižených lidí se zdvojnásobí každých dvacet let. Odhaduje se, že v současné době je demencí postiženo na celém světě kolem 70 milionů lidí. Pacientů s Alzheimerovou chorobou je tak více než pacientů s rakovinou prsu a rakovinou prostaty dohromady. Občas blikne jiskřička naděje s novým lékem, ale tu obvykle uhasí nepřesvědčivé výsledky klinických testů spolu s nežádoucími vedlejšími účinky. Objevily se krevní testy, které usnadňují časnou diagnostiku Alzheimerovy choroby, ale bez spolehlivé a účinné léčby je taková diagnóza jen stvrzením průšvihu, pro který nemáme řešení.
Nová metoda léčby vyvinutá týmem pod vedením Marca Colonny z Washington University School of Medicine v americkém St. Louis využívá principu CAR terapie. Tento postup se už prosadil při léčbě leukémií a nově se osvědčuje např. při boji s autoimunitními onemocněními. Využívá umělého genu, podle kterého si buňky imunitního systému vytvoří na svém povrchu tzv. chimerický antigenový receptor (odtud je i zkratka CAR). Buňky imunitního systému se pak přes tento receptor vážou na strukturu, která je příčinou choroby. V případě leukémií to jsou leukemické bílé krvinky.
Velkou nevýhodou CAR terapií je, že pro léčbu jsou používány pacientovy buňky a ty se musí pro každého nemocného připravit zvlášť. Je to drahé. Příprava buněk pro jednoho pacienta vyjde na 400 tisíc dolarů. Hledají se cesty ke zlevnění, a i tady se blýská na lepší časy. Indičtí vědci dokázali stlačit cenu přípravy léčebných buněk na 40 000 dolarů a věří, že je možné buňky připravit i při polovičních nákladech.
Dnes se ale nabízí alternativní přístup, a tím je modifikace buněk imunitního systému přímo v těle pacienta, a to buď prostřednictvím geneticky upraveného viru nebo molekulárního nástroje genového inženýrství neseného lipidovými nanočásticemi (podobné částice jsou nosičem mRNA vakcíny proti SARS-CoV-2). A právě o to se pokusili Colonna a spol. ve studii publikované vědeckým časopisem Science.
Cílem je amyloid-beta
Pro Alzheimerovu chorobu je typické hromadění amyloidu-beta v mezibuněčných prostorech mozku. Tím se spouští celá kaskáda nežádoucích procesů. V mozku se rozhoří zánět, v neuronech se hromadí shluky proteinu tau a výsledkem je odumírání neuronů. Amyloid-beta je považován za spouštěč onemocnění, a proto se na něj soustředí značná část vyvíjených léčebných postupů. Colonna a jeho spolupracovníci nasměrovali proti amyloidu-beta buňky mozku známé jako astrocyty. Pro tento účel vybavili tyto buňky speciálně konstruovaným chimérickým antigenovým receptorem.
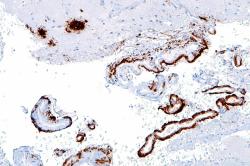
Astrocyty jsou řazeny ke gliovým buňkám, kterých máme v mozku zhruba stejné množství jako neuronů. Plní zde pestrou paletu úloh. Astrocyty slouží jako klíčové regulátory neuronálních funkcí. Poskytují neuronům nezbytnou metabolickou podporu, modulují uvolňování neurotransmiterů a udržují zdraví neuronů. Jsou schopny fagocytózy a mohou tak z mozku odstraňovat nežádoucí látky. Colonnův tým chtěl odzkoušet, zda lze astrocyty donutit také k hltání amyloidu-beta.
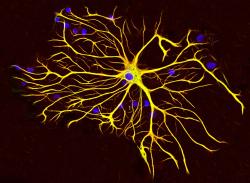
Pro modifikaci astrocytů a vytvoření chimérického antigenového receptoru namířeného na amyloid-beta zvolili Colonna a spol. geneticky modifikovaný virus, konkrétně adenoasociovaný virus, který patří k oblíbeným nástrojům současných genových terapií. Záměr vědcům vyšel. Díky výbavě chimerickým antigenovým receptorem dokázaly astrocyty pohlcovat amyloid-beta a čistit od něj mozek.
Ne tak úplně uzdravené myši
Vědci z Colonnova týmu vpíchli dávku geneticky modifikovaného viru vybaveného genem pro chimérický antigenový receptor laboratorním myším do cév za okem. Pro pokus vybrali zvířata, kterým se v mozku hromadí amyloid-beta a výsledkem je onemocnění analogické Alzheimerově chorobě. Gen přenášený modifikovaným virem byl upraven tak, aby fungoval pouze v astrocytech. Pokud by ho virus zanesl do jiných buněk mozku, chimerický antigenový receptor by se v nich nevytvořil.
Virus pronikl z krevního řečiště myší do mozku, což není úplně samozřejmé. Stěny cév v mozku jsou pro mnoho látek i mikrobů neprostupné a vytvářejí tzv. hematoencefalickou bariéru. Ta chrání mozek před průnikem škodlivin i původců infekčních chorob, ale pro léčbu představuje nepříjemnou překážku, která se staví léku do cesty. Virus dokázal dodat do astrocytů gen pro chimerický antigenový receptor a astrocyty vybavené tímto receptorem se pustily do díla. Likvidovaly myším v mozku amyloid-beta a mozek devastovaný obdobou lidské Alzheimerovy choroby dramaticky ozdravily.
Likvidace amyloidu-beta nebyla jedinou změnou k lepšímu. V důsledku léčby došlo také ke „zklidnění“ buněk mozku známých jako mikroglie. Ty patří ke strážcům zdraví mozku. Při Alzheimerově chorobě jsou ale mobilizovány tak silně, že jejich přehnané akce napáchají více škod než užitku. Když se vědci dříve pokoušeli léčit Alzheimerovu chorobu protilátkami, jež se vážou na amyloid-beta, docházelo k eskalaci aktivity mikroglií a dalšímu poškozování mozku.
##seznam_reklama##
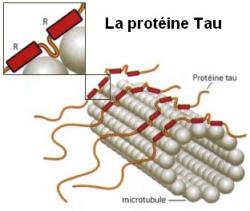
CAR terapie nebyla schopna myši z obdoby Alzheimerovy choroby zcela vyléčit. To potvrzuje, že amyloid-beta zřejmě není jediný „škůdce“. Dalším kandidátem je protein tau, jehož hromadění v neuronech je nastartováno tvorbou shluků amyloidu. K dispozici jsou už chimerické antigenové receptory cílené na protein tau. Dá se proto předpokládat, že kombinovaná CAR terapie nasměrovaná jak proti amyloidu-beta, tak i proteinu tau, přinese lepší výsledky. Na to si však budeme muset ještě nějakou dobu počkat. Každopádně se CAR terapie ukazuje jako nadějný způsob léčby Alzheimerovy choroby.
Prameny:
Barthélemy, N. R., et al. (2024). Highly accurate blood test for Alzheimer’s disease is similar or superior to clinical cerebrospinal fluid tests. Nature Medicine, 30(4), 1085-1095.
Boles, J., & Gate, D. (2026). Astrocytes engineered to fight Alzheimer’s plaques. Science, 391(6789), 990-991.
Chen, Y., et al. (2026). Targeting amyloid-β pathology by chimeric antigen receptor astrocyte (CAR-A) therapy. Science, 391(6789), eads3972.
Rehman, M. A., & Arshad, H. (2024). A discount on the cost of cancer: India's homegrown CAR-T cell therapy. Blood Cell Therapy, 7(4), 121.
Van Dyck, C. H., et al. (2023). Lecanemab in early Alzheimer’s disease. New England Journal of Medicine, 388(1), 9-21.
Zhang, N., et al. (2025). Development of an in situ CAR-T cell protocol through optical and PSMA-targeted PET imaging. Proceedings of the National Academy of Sciences, 122(24), e2504950122.
Redakce si dovolila připojit záznam nejnovějšího autorova pokecu s Markem Špinkou o DNA,...
A ještě jedno starší v Café Nobel
