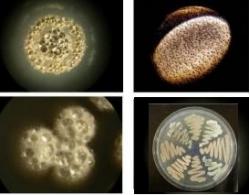
Vědci vedení Gerardem Wrightem zkoumali citlivost k antibiotikům u 480 kmenů bakterií patřících k aktinomycetám z rodu Streptomyces. Tuhle bakteriální "zoo" si pořídili celkem snadno - izolovali je z půdy. Výsledky jejich šetření zveřejněné v prestižním vědeckém týdeníku Science nahání lékařům husí kůži.

Všechny zkoumané kmeny odolávaly hned několika různým antibiotikům. Některé vzdorovaly dokonce patnácti z jednadvaceti testovaných léků.
O tom, že je půdní mikroflóra ve svých schopnostech vzdorovat antibiotikům skutečně vynalézavá svědčí fakt, že 480 zkoumanými kmeny našli vědci 200 různých "profilů odolnosti" k lékům. "Portfolio" rezistentních genů má skoro každý mikrob jiné, své vlastní.
Wright a jeho kolegové hovoří v souvislosti s pestrým spektrem genů zajišťujících bakteriím odolnost k antibiotikům o "půdním rezistomu". Tenhle termín budeme slýchat zřejmě stále častěji, protože z pesrého repertoáru půdních bakterií čerpají i původci lidských a zvířecích chorob.
Kanadští vědci prověřovali citlivost půdních mikroorganismů jak proti tradičním antibiotikům (např. erytromycin), tak ke zcela novým preparátům, které byly teprve nedávno schváleny k léčbě (např. telitromycin či tigecyklin). Mezi testovanými léky figurovaly látky přirozeně produkované půdní mikroflórou (např. vankomycin), dále pak polosyntetické deriváty vzniklé ve farmaceutických provozech pozměněním "přírodních" antibiotik (minocyklin a cefalexin) a nakonec i antibiotika "syntetická", jejichž obdobu z přírody neznáme (ciprofloxacin a linezolid).
Některá antibiotika byla neúčinná prakticky ke všem testovaným kmenům. Největším překvapením byla v tomto směru častá rezistence k daptomycinu povolenému teprve nedávno pro léčbu kožních infekcí a infekcí měkkých tkání. Plných 80% prověřovaných kmenů inaktivovalo v živné půdě veškerý daptomycin během 48 hodin. Je jasné, že bakterie používají pro zneškodnění tohoto léku hned několika různých mechanismů. Původci lidských onemocnění tyhle triky neumějí - zatím.
Plná polovina testovaných mikrobů byla vybavena enzymy pro rozklad antibiotika rifampicinu hojně užívaného k léčbě infekcí bakteriemi z okruhu původce tuberkulózy. Tento mechanismus rezistence mikrobiologové zatím neznali. Původce tuberkulózy získává rezistenci k rifampicinu bodovou mutací genu pro cílový enzym RNA polymerázu.
Rezistenci k antibiotikům by nás neměla u aktinomycet rodu Streptymyces překvapovat. Mezi těmito bakteriemi najdeme polovinu producentů antibiotik využívaných současnou medicínou. Aktinomycety jsou proto vybaveny i geny, které je chrání před účinky jimi produkovaných antibiotických látek. Těmito geny vedou bakterie čilý "směnný obchod". Jsou s to přijmout úseky DNA z uhynulých mikroorganismů a s nimi tak získávají i nejrůznější geny. O osudu takto získaného genu rozhoduje do značné míry prostředí, v jakém bakterie žije. Pokud se s novou genovou akvizicí domůže významné výhody, má genetická inovace cestu k šíření otevřenu dokořán.
A tady vstupuje do hry člověk. V životním prostředí končí naším přičiněním obrovské množství antibiotik nebo molekul vzniklých jejich částečnou degradací či metabolismem. Jejich zdrojem je humánní i veterinární medicína a zemědělství. Pokud se tyto látky dostanou do půdy, působí na tamější bakteriální společenství silným selekčním tlakem, s kterým se nejlépe vypořádají nově vznikající rezistentní kmeny.

Tento scénář vzniku rezistence podpořil nález půdních bakterií odolných proti syntetickým antibiotikům. Kanadská studie prokázala u 52 kmenů rezistenci k ciprofloxacinu používanému k léčbě infekcí močového ústrojí. V půdě žijí kmeny bakterií vzdorující také dalšímu z testovaných syntetických antibiotik linezolidu, jenž je využíván proti multirezistentním kmenům enterokoků, stafylokoků a pneumokoků.
Cesty, jakými se může rezistence z půdních bakterií přenášet na patogenní mikroorganismy, nejsou podrobněji prozkoumány. Jak spletité jsou, dokazuje možný scénář vzniku rezistence k vankomycinu u původce závažných infekcí "zlatého stafylokoku" Staphylococcus aureus.
Od roku 1997 jsou známy kmeny S. aureus odolné k vankomycinu díky mutaci. Tyto kmeny vzdorují vankomycinu až do koncentrací 12 mikrogramů na mililitr. V roce 2002 se poprvé objevily kmeny S. aureus, které získaly geny pro inaktivaci vankomycinu výpůjčkou na bakteriální genové burze. Pilíř tohoto typu rezistence tvoří geny vanH, vanA a vanX pocházející z aktinomycet, které vankomycin přirozeně produkují a musí se proti jeho účinkům chránit. Geny vanH, vanA a vanX zajišťují přežívání bakterií Staphylococcus aureus i při koncentracích vankomycinu nad 500 mikrogramů na mililitr.

Selekční tlak, který zajistil vyšší evoluční úspěšnost bakterií rezistentních k vankomycinu, má na svědomí člověk. Evropští zemědělci přidávali do krmiv hospodářským zvířatům derivát vankomycinu avoparcin. Zkrmování antibiotik je dnes zakázáno, ale ještě zcela nedávno zemědělci tímto způsobem "preventivně čistili" svá zvířata od choroboplodných bakterií a zajišťovali si tak vyšší rentabilitu živočišné produkce. O antibioticích hovořili eufemisticky jako o "stimulátorech růstu".
Následky tohoto nezodpovědného počínání na sebe nedaly dlouho čekat. Zvířata krmená avoparcinem měla ve výkalech enterokoky, které vzdorovaly nejen avoparcinu, ale i vankomycinu určenému přednostně pro použití v humánní medicíně. Geny pro odolnost k vankomycinu získaly ne zcela jasným způsobem enterokoky vyvolávající střevní infekce u člověka. První epidemie vyvolané rezistentními enterokoky byly podchyceny v 90. letech dvacátého století v USA. V následujících deseti letech si geny pro rezistenci k vankomycinu našly cestu do dědičné informace bakterie S. aureus. Rozhodující geny zřejmě získal v těle pacienta se silně oslabenou imunitou, který měl vřed infikovaný současně jak stafylokokem, tak i bakteriemi rezistentními k vankomycinu.
Wright a jeho spolupracovníci vidí v půdních rezistentních bakteriích silně podceňovaný zdroj genů, z kterého mohou horizontálním transferem získávat rezistenci i patogenní mikroorganismy. V řadě případů jde o zcela nové a u patogenů doposud neznámé typy rezistence. Wright upozorňuje na fakt, že zřejmě podchytil jen příslovečnou "špičku ledovce", protože mohl studovat jen bakterie, které lze kultivovat v laboratorních podmínkách. Existují přesvědčivé důkazy o tom, že geny pro rezistenci k antibiotikům mají ve svých genomech i bakterie, jež se kultivaci vzpírají. Navíc se autoři studie zabývali jen případy silné rezistence a její mírnější projevy nezkoumali. Z dnešního hlediska "exotické" mechanismy, jimiž dosahují rezistence půdní mikroorganismy, se mohou v budoucnu objevit i u choroboplodných bakterií významných z hlediska humánní či veterinární medicíny.
Wright doufá, že poznatky o mechanismech rezistence půdních mikrobů najdou uplatnění při vývoji nových antibiotik. Podle Wrighta nám otevírají možnost kombinovat léčbu pomocí antibiotik s podáváním látek potlačujících účinky těch bakteriálních enzymů, jež rezistentní patogenní bakterie k inaktivaci antibiotik využívají.

… nebo takhle …

… a nebo dokonce takto.
Pramen: Science, Medical Tribune
Diskuze: