Úvodem několik slov o inzulínu
Inzulín je hormon tvořený B buňkami v Langerhansových ostrůvcích ve slinivce břišní. Snižuje hladinu cukru v krvi a jeho sekrece se řídí hladinou glukózy v krvi. Čím je více glukózy, tím více inzulínu slinivka produkuje.
Takže, když si dáme rohlík, amyláza ze slin škrob (polysacharid) naporcuje na oligosacharidy. Těch se ve střevě ujme amyláza pankreatická a protože má na štěpení více času, zkrátí je až na disacharidy. Ty jsou už dostatečně titěrné, aby prošly sliznicí střeva, kde sedají do práce enzymy maltáza se sacharázou a výsledkem jejich snažení jsou monosacharidy – glukóza. Ta už prochází do krevního řečiště, aby svou energetickou hodnotou potěšila buňky od palce u nohy po ty nervové v mozku. Jenže bez inzulínu není glukóza buňkám nic platná. Až v jeho přítomnosti, když se naváže na jejich receptory, buňky otevřou své „brány“ a glukóza (přes kaskádu pomocníků) začne proudit do nitra buněk.Tam jí pak čeká osud paliva. Z přebytků se pro horší časy vyrobí glykogen.
Za delší dobu po jídle začne být glukózy v krvi málo, slinivka sníží tvorbu inzulínu. Bez jeho signálů buňky svá stavidla pro příjem uzavřou. Když zlé časy trvají, přijdou na řadu rezervy glykogenu. Játra ho rozloží na glukózu a její nárůst v krvi spouští sekreci inzulínu. Ten otevře buňkám stavidla a ty se znovu napakují energií. A tak to jde stále dokola. Svaly povzbuzené inzulínem si mohou začít vydělávat na chleba prací, a tukové buňky tvořit tuk (proto se při diabetu typu 2, kdy je krvi vyšší hladina inzulínu, tak snadno tloustne).
Co je diabetes druhého typu?
V podstatě jde o inzulínovou rezistenci. To slovo rezistence znamená, že buňky přestávají být schopny s inzulínem komunikovat a chovají se, jako by nebyl. Škodí si tím, protože i když je v krvi glukózy dost, je pro ně nedostupná. Tím, že glukózu využívají buňky omezeně, její koncentrace v krvi stoupá. Stoupá-li krevní cukr, buňky slinivku to nutí produkovat více inzulínu. Proto diabetikům roste v krvi nejen hladina cukru, ale i inzulínu. Jde o poruchu a ta se časem někde projeví.
Jak do toho zapadá rakovina?
Záněty jsou záležitostí imunitního systému a bílých krvinek. Je to boj a k němu je potřeba energie, hodně energie a tak se imunitní systém pomocí cytokinů, což je taková psaná řeč buněk, domluví s dalšími buňkami, že je třeba mobilizovat energetické rezervy. Dostatek glukózy ale rakovinovým buňkám vyhovuje. Tukové tkáni také, ta je navíc místem, kam se v případě léčby pomocí cytostatik dostává lék obtížně. Zvrhlé buňky v ní nacházejí řadu schovek a tak i po léčbě se choroba z těchto míst ráda znovu vrací. Hlad rakovinových buněk po glukóze je tak velký, že ho lze využít k detekci. Pokud se na glukózu použije izotop, nebo se jinak označí, místa s vysokou spotřebou (nádory) se na obrazovce monitorů rozsvítí.

Hypotéza
Leukemické (rakovinové) buňky jsou nenažrané a chovají se ke svým zdravým kolegyním macešsky. Značnou část glukózy z krve vychytávají jen pro sebe. Ale co když nejen to. Co když jdou ve své sobeckosti ještě dál a navozují zdravým buňkám inzulínovou rezistenci? Znesnadňují zvrhlé buňky využití energie svým zdravým kolegyním, aby v krvi bylo glukózy co nejvíc jen pro ně? Tak právě to se američtí výzkumníci pokusili zjistit.
K testům na ověření hypotézy, v níž přiřkli rakovinovým buňkám zvlášť zavrženíhodnou povahu, si vědci přizvali leukemické myši. Ty se vyznačují sklonem k obezitě, jejich tuková tkáň je místem zánětů i rezervoárem zvrhlých buněk. Pokus ukázal, že z míst zánětu s leukemickými buňkami se šíří cytokiny. A že ty skutečně zdravým buňkám navozují inzulínovou rezistenci. Jinak řečeno, myším nemocným leukémií se zvyšuje hladina krevní glukózy a normální zdravé buňky přestávají být schopny využít. To znamená, že rakovina zdravým buňkám navozuje stav, v jakém jsou buňky nemocných s diabetem druhého typu.
Dalším krokem byl pokus, v němž svým korpulentním nemocným svěřenkyním dodali inzulín. To jejich zdravým buňkám strádání z nedostatku energie do značné míry vylepšilo. Tím nejzajímavějším poznatkem na tom bylo, že zatímco zdravým buňkám to vracelo chuť do života, leukemickým buňkám to žádnou výhodu nepřineslo, naopak. Nejspíš proto, že jejich metabolismus a s tím spojená chamtivost po energii, je vystupňovaná na maximum a i když zvýšená hladina cukru jej činí dostupnějším, neprofitují z toho.
Vyhladovění rakoviny
Pokus s dodáním inzulínu mění široce zakořeněnou představu, že rakovinu je dobré připravit o živiny, například tím, že u nemocného léky potlačíme produkci inzulínu, čímž leukemickým buňkám omezíme dostupnost glukózy v krvi. Ukazuje se, že snahy přibrzdit leukémii tímto způsobem nejsou správné a že opak nejspíš bude pravdou. Ze záměrně zvýšené hladiny inzulínu a větší dostupnosti glukózy totiž těží především zdravé buňky a ty ke svému fungování organismus potřebuje. Dovoluje mu to lépe se bránit. Svědčí o tom myši léčené podporou inzulínu, v nichž se leukemické buňky nemnožily tak agresivně, jako v těch, kterým se extra porce inzulínu nedostalo. Že tento přístup bude ten správný, naznačilo i to, že došlo k přidušení tvorby leukemických buněk v periférii i v kostní dřeni. Zlepšení stavu nemocných následkem přilepšení inzulínem se projevilo i tím, že méně hubly. Nyní se ale vrátíme k té části výzkumu, která se věnovala leukemickým buňkám z pohledu jejich schopnosti to nějak zaonačit, aby tkáně hostitele postihla inzulínová rezistence.
Jak to dělají?
Tukové buňky byly dlouho považovány za metabolicky neaktivní, sloužící jen jako rezervoár přebytečně přijaté energie. Pak ale byly objeveny adipokiny – látky, které tukové buňky (adipocyty) produkují. Nyní už jich známe desítky. Jsou to látky proteinové povahy a buňky je vyplavují do krevního oběhu a s jejich pomocí dovedou zařizovat celou řadu funkcí. Ovlivňují příjem potravy, výdej energie, rozpoutání zánětu i razantnost imunitní reakce. Kromě toho stojí za patologickými komplikacemi kardiovaskulárního systému. A jakoby toho nebylo málo, tak i za selháním funkcí pohlavního systému.
Také v případě leukémii hraje tuková tkáň neblahou úlohu
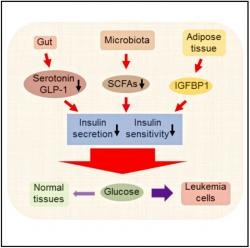
Špekovité faldy produkují protein IGFBP1. Ten není lékařům neznámý. Dříve mu říkali placentární protein. V našem případě se ukázalo, že zhoršuje vyhlídky nemocného. Zajímavé na tom je, že leukemické buňky se o produkci tohoto proteinu samy přičiňují. Není divu, jeho cílem jsou zdravé buňky hostitele - snižuje jim citlivost na inzulín. Tkáně tak jeho zásluhou začnou mít problém s příjmem glukózy. Dělá to dojem, jakoby zmíněný protein se z nějakého důvodu snažil v organismu zavést šetření glukózou, ale činí tak na nesprávném místě a v nejméně vhodnou dobu, a tak z klání s rakovinou vychází vítězně buňky nádoru, zatímco zdravé tkáně chátrají.
Poznatku o škodlivosti proteinu IGFBP1 se vědci pokusili vytěžit
Provedli pokus, v němž molekuly zloducha znefunkčnili. Udělali to tak, že na něj "pustili jiný protein" – protilátku připravenou tak, aby se navazovala na jeho funkčně důležité místo a zakryla ho. Takto nalepenými záplatami protein IGFBP1 připravili o jeho fyziologickou aktivitu. Pokus se uskutečnil na živých myších a těm se ulevilo. Leukemickým myším pacientům to prospělo hned ve dvou směrech. Jednak buňky ve zdravých tkání přestaly být ke glukóze netečné a opět nabyly schopnost ji lépe využívat. Zároveň ale eliminace proteinu myškám zvýšila hladinu inzulínu, což prospělo všem buňkám, ale těm zdravým mnohem víc. I když se leukemii u myší tímto způsobem vyléčit nepodařilo, podáním protilátky proti zlému proteinu IGFBP1 se zvrhlé leukemické buňky dařilo do značné míry dlouho držet na uzdě. Ošetřeným myškám se celkový zdravotní stav zlepšil a také z nich nebyla tak rychle kost a kůže, jako z vrstevnic, v nichž leukemie řádila plnou silou.
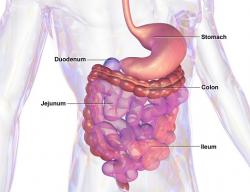
Leukemie je komplexní onemocnění
Pokusy v laboratořích Denverské nemocnice ukázaly, že leukemie do značné míry souvisí s procesy, které jsme dosud spojovali s diabetem. Kromě toho ozřejmily i jakou úlohu vtom hraje zažívací trakt. Konkrétně jde o mikrobiom, někdy přezdívaný „naše druhé já“, protože bez mikrobů bychom umřeli hladem. Jak už to tak bývá, v každé komunitě se najdou příživníci, kteří jen škodí. Ty umravňuje imunitní systém. I když je hranice mezi zdravím a nemocí dost nepřehledná, tamní dění spolurozhoduje jak co do vzniku diabetu, tak i leukemie i otylosti. Dokazují to i dřívější pokusy s transplantacemi fekálií. Smradlavou transplantací již mnohde léčí některé problémy s imunitou a nutno říci, že úspěšně. Právě u těchto případů vyšlo najevo, že když se exkrementy z tlouštíka přenesou hubeňourovi, tak začne nezdravě tloustnout. Nejspíš proto, že takové případy Denverským nebyly neznámé, další svůj pokus směrovali na mikrobiom. Vyzkoušeli, zda transplantace mikrobiomu také ovlivní to, co je pro nemocné leukémií a diabetiky společné – sníženou senzitivitu buněk na inzulín.
Jak dopal přenos obsahu střeva z leukemických myší do zdravých?
Předpoklad se naplnil. Zdravým myškám to navodilo snížení citlivosti buněk na inzulín a následně došlo i na zvýšení hladin krevního cukru a inzulínu. Právě to jsou ukazatele, které signalizují jak zhoršování cukrovky, tak i prospívání leukemických buněk.
Jak to je možné?
Když do našeho vysvětlování přizveme genetiku, rázem to přestane být tak nelogické. To, co po rodičích dědíme, se nám montuje do řady věcí. U myší náchylných k leukemii to je to samé. I ony mají celou řadu genů, které je činí k rakovině náchylnější. Mezi takové patří i ty geny, které jim dávají do vínku zkrácené střevo. To pochopitelně výrazně mění složení mikrobiomu. A protože se složení mikrobiomu plete jak do imunity, tak i do výživy, neměly by nás už překvapit výsledky pokusů, při nichž se přenesením mikrobiomu od zdravých dárců nemocným a od nemocných zdravým daří zdravotní stav ovlivnit žádoucím, respektive nežádoucím směrem ve prospěch vzniku nemoci.
Model je model ale co člověk?
Pokud by šlo jen o poznatek na myších, bylo by to k ničemu, a tak v Denveru došlo i na pokusy na lidech. Přesněji, na jejich krevních buňkách. Ukázalo se, že nemocní akutní leukemií měli v krvi (v porovnání se zdravými), dvacetkrát více zlého proteinu IGFBP1. Ti, kteří měli „jen“ myelodysplastický syndrom (ten bývá označován za předstadium leukemie), ho tolik neměli. Nemocní s tímto syndromem na tom byli s produkcí zlého proteinu mezi zdravými a těmi s rakovinou zhruba uprostřed. To mimo jiné znamená, že zmíněný protein se ukazuje být dobrým markerem vypovídajícím, jak na tom ten který pacient je. Jak další pokusy ukázaly, dají se podle hladiny přesně zjistit i stavy remise nemoci (a tedy i možnost ubrání na razantnosti léčby).
Nových poznatků je celá přehršel
Zlý protein odhalil, že metabolické změny pozorované u myší, jsou společné myším i nám. Že jsou to právě leukemické buňky, kdo navozuje zdravým buňkám svého hostitele inzulínovou rezistenci. Nyní známe i regulační mechanismus, který s pomocí cytokinů rakovinu a diabetes spojuje.
Víme, jak se intrikánským leukemickým buňkám daří prosadit, aby se zdravé buňky staly k inzulínu netečné a přišly tak o schopnost využívat glukózu.
Že významnou úlohu v patogenézi hraje tuková tkáň produkcí proteinu IGFBP1.
Že jeho vysoká hladina v krvi je nejen známkou rezistence tkání k inzulínu, ale též prognózou dalšího zhoršení stavu, neboť snižuje nejen produkci inzulínu v pankreasu, ale i jeho uvolňování do krve. Významným poznatkem je, že se zlý protein zdařilo protilátkou vyblokovat a že to myším pacientům prospělo.
Pokusy také ukázaly na významnou roli mikrobiomu, což do jisté míry vysvětluje, proč se u lidí pozoruje souvislost mezi onemocněním tlustého střeva a vyšším rizikem leukemie a cukrovky. Autoři studie to vysvětlují tím, že změněný mikrobiom produkuje toxiny vyvolávající lokální záněty. Ty se prostřednictvím krve šíří dál a postupně dávají vznik systémovému zánětlivému stavu. Jeho veličenstvo mikrobiom nám dává jasně na srozuměnou, jak mocně umí promlouvat do glukózového metabolismu a podílet se na vzniku chorob, v nichž hraje úlohu inzulínová rezistence.
Poodhalení úlohy proteinu tukové tkáně IGFBP1, kterému jsme zde říkali „zlý protein“, a jehož eliminací se kolektivu Haobin Ye podařilo výrazně stav nemocných myší zlepšit, je dalším krůčkem ke světlým zítřkům, v nichž choroby jako leukemie a diabetes zmizí v propadlišti dějin.
Literatura
Haobin Ye, et al.: Subversion of Systemic Glucose Metabolism as a Mechanism to Support the Growth of Leukemia Cells, Cancer Cell (2018). DOI: 10.1016/j.ccell.2018.08.016
Personalizovaná transplantace stolice tlouštíkům
Autor: Josef Pazdera (09.10.2017)
Diabetikom nestačí len liečba cukrovky
Autor: Matej Čiernik (22.12.2017)
Odhalena další příčina cukrovky
Autor: Dagmar Gregorová (07.06.2018)
S křešinou k oltáři i na cukrovku
Autor: Josef Pazdera (16.09.2018)
Slibná léčba cukrovky lepidlem
Autor: Josef Pazdera (28.09.2018)
Diskuze: